Металлы представляют собой уникальный класс материалов, обладающих рядом выдающихся физических и структурных особенностей. Одна из главных характеристик металлов - их высокая плотность. Объяснить этот феномен можно с помощью физических законов и особенностей структуры металлической решетки.
Во-первых, металлы обладают свободными электронами в своей электронной оболочке, что является одной из причин их высокой плотности. Большое количество свободных электронов позволяет металлам легко проводить электрический ток и тепло, что делает их ценными для использования в различных промышленных отраслях.
Во-вторых, структура металлической решетки также влияет на их плотность. Металлы имеют кристаллическую структуру, в которой атомы регулярно расположены и сильно связаны друг с другом. Благодаря этому, металлы обладают высокой плотностью и прочностью.
Кроме того, на плотность металлов также оказывает влияние их атомная масса. Чем выше атомная масса металла, тем выше его плотность. Атомы металлов обычно тяжелее атомов неметаллов, что является еще одной причиной их плотности.
В целом, плотность металлов обусловлена их свободными электронами, кристаллической структурой и атомной массой. Понимание физических и структурных особенностей металлов является ключевым для их применения и разработки новых материалов с улучшенными свойствами.
Плотность металлов: причины и свойства

Металлы - это материалы, обладающие высокой плотностью, то есть значительным количеством массы, занимающим относительно небольшой объем. Почему так происходит?
Одной из причин высокой плотности металлов является их атомная структура. В металлической решетке атомы располагаются плотно и регулярно, образуя кристаллическую решетку. Между атомами находятся электроны, которые свободно перемещаются по всей решетке. Благодаря этому свободному движению электронов, металлы обладают высокой электропроводностью и теплопроводностью, а также способностью к пластичности и деформации.
Еще одной причиной высокой плотности металлов является их атомная масса. Атомы металлов обычно имеют большую массу, чем атомы других элементов, что приводит к более высокой плотности материала. Например, атом железа имеет массу около 56 атомных единиц, в то время как атом кислорода - всего лишь около 16 атомных единиц. Поэтому сплавы с содержанием металлов обычно имеют более высокую плотность, чем сплавы без металлов.
Некоторые металлы также обладают особенностями в атомной структуре и связи между атомами, которые также влияют на их плотность. Например, чугун - один из самых плотных металлов - имеет свою специфическую кристаллическую решетку, что делает его значительно более плотным, чем сталь или алюминий.
Важно отметить, что плотность металлов может быть изменена в зависимости от условий. Например, изменение температуры или примесь других элементов может влиять на плотность металла. Кроме того, плотность металла может быть изменена путем обработки его сплавами или применения специальных технологий, например, прокатки, отливки или спекания.
Почему металлы такие плотные?

В своей природе металлы обладают высокой плотностью по нескольким причинам. Во-первых, металлы характеризуются высокой атомной плотностью. Атомы в металлах располагаются близко друг к другу и образуют кристаллическую решетку, что способствует увеличению плотности материала.
Во-вторых, металлы обладают большим количеством внутреннего энергетического потенциала. Это объясняется наличием свободных электронов в их структуре. Свободные электроны способствуют хорошей электропроводности металлов и способны образовывать силовые поля, которые притягивают атомы друг к другу и увеличивают плотность материала.
Также, металлы обладают особым механизмом связи атомов - металлической связью. В этом случае, электроны между атомами могут двигаться свободно, что позволяет им принимать участие в формировании плотной и устойчивой структуры материала. Благодаря этому, металлы обладают высокой плотностью.
В целом, плотность металлов определяется не только их химической структурой, но и другими факторами, включая атомную решетку, наличие свободных электронов и связь между ними. Эти особенности вместе способствуют высокой плотности металла и его уникальным физическим свойствам.
Физические свойства металлов, влияющие на плотность
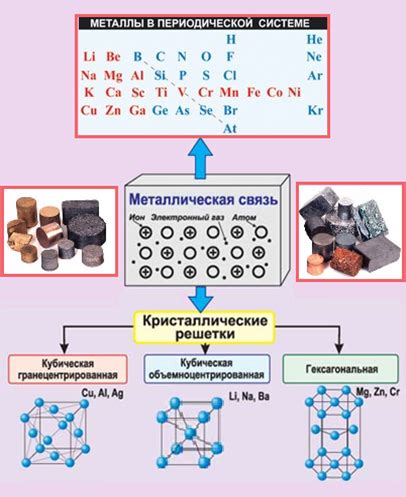
Металлы обладают рядом физических свойств, которые влияют на их плотность.
Во-первых, атомы металлов имеют плотную упаковку в кристаллической решетке. У металлов атомы расположены близко друг к другу и образуют компактную структуру, что способствует увеличению плотности. Например, у железа и алюминия атомы упакованы в кубическую решетку, что делает их особенно плотными.
Во-вторых, металлы обладают высоким атомным числом, то есть у них большое количество атомов в единице объема. Это также влияет на увеличение плотности материала. Например, у свинца атомное число равно 82, что делает его одним из самых плотных металлов.
Кроме того, металлы часто образуют сплавы, в которых присутствуют различные элементы. Назначение сплава может быть разнообразным: повышение прочности, улучшение рабочих характеристик, изменение цвета и т.д. Однако при создании сплава плотность металла может измениться в зависимости от его состава.
Таким образом, разные физические свойства металлов, такие как упаковка атомов в кристаллической решетке, высокое атомное число и образование сплавов, вносят свой вклад в общую плотность металлического материала.
Структурные особенности металлов и их влияние на плотность

Металлы обладают уникальными структурными особенностями, которые влияют на их плотность. В основе структуры металлов лежит кристаллическая решетка, которая организована в определенном порядке.
Кристаллическая структура металлов характеризуется высоким уровнем упорядоченности атомов, что обеспечивает их плотную укладку. Атомы металла образуют регулярные пакеты, называемые кристаллическими зернами, которые продолжаются в трех измерениях.
Еще одной важной особенностью структуры металлов являются свободные электроны, которые располагаются между атомами. Эти электроны формируют так называемое "море электронов", которое служит связующим элементом между атомами и придает металлам специфические электрические и теплопроводящие свойства.
Все эти факторы, такие как упорядоченность атомов, наличие свободных электронов и их взаимодействие, способствуют образованию твердой и плотной структуры металлов. Именно благодаря этим особенностям металлы являются плотными материалами.
Взаимное расположение атомов в металлической решетке
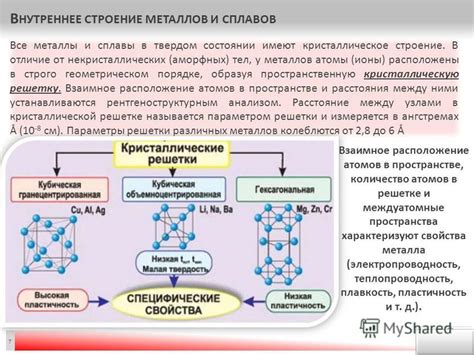
Металлы являются плотными из-за особенностей их структуры. В металлической решетке атомы размещены в кристаллической структуре, которая обеспечивает взаимосвязь и компактное расположение атомов.
В металлической структуре атомы металла образуют кристаллическую решетку, состоящую из регулярно повторяющихся элементов. В каждом элементе решетки атомы располагаются вблизи друг друга, образуя кристаллическую структуру.
Взаимное расположение атомов в металлической решетке характеризуется тремя основными параметрами: атомным радиусом, интератомным расстоянием и координационным числом.
Атомный радиус определяет размер атома металла и зависит от его химического состава и структуры. Интератомное расстояние - это расстояние между соседними атомами в решетке металла. Оно обычно меньше суммы атомных радиусов и определяет компактность решетки.
Координационное число показывает, сколько атомов окружает каждый атом в решетке. В металлических решетках координационное число обычно составляет 6 или 8, что способствует плотному упаковке атомов и высокой плотности металла.
Кристаллическая структура и плотность металлов
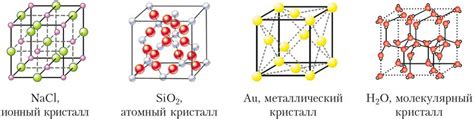
Кристаллическая структура является одной из основных причин, почему металлы обладают высокой плотностью. Металлы имеют относительно регулярную структуру, состоящую из слоев атомов или их кристаллических решеток, которые тесно упаковываются друг к другу. Это создает компактную сетку, которая способствует высокой плотности металла.
Кристаллическая структура металлов обычно представляет собой кубическую решетку или гексагональную плотную упаковку атомов. В кубической решетке каждый атом окружен шестью соседними атомами, что обеспечивает наиболее плотное упаковывание. Гексагональная плотная упаковка также обладает высокой степенью плотности, но у нее два различных вида слоев атомов.
Плотность металлов также зависит от их химического состава. Различные металлы имеют разные атомные и ионные радиусы, что может влиять на их плотность. Например, металлы с большими атомными радиусами ищутся в кристаллическую решетку, что приводит к увеличению плотности. Кроме того, на плотность металлов может влиять наличие дополнительных включений, которые либо уменьшают, либо увеличивают плотность материала.
Интерметаллические соединения также могут влиять на плотность металлов. Когда два металла образуют соединение, их атомы образуют новую кристаллическую структуру. Плотность такого интерметаллического соединения может быть значительно выше или ниже, чем у отдельных металлов до образования соединения.
Химический состав и плотность металлов
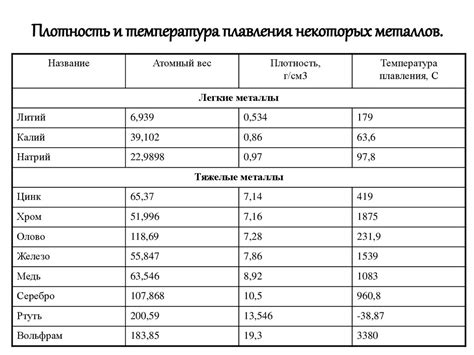
Металлы - это класс веществ, обладающих определенными физическими и химическими свойствами. Один из ключевых параметров, определяющих их характеристики, является плотность. Плотность металлов зависит от их химического состава и кристаллической структуры.
Все металлы имеют атомную структуру, в которой положительно заряженные атомы расположены в кристаллической решетке. Однако различные металлы имеют разные кристаллические структуры, что приводит к различиям в их плотности. Например, медь, имеющая кубическую решетку, имеет плотность около 8,96 г/см³, в то время как алюминий, с гексагональной или кубической решеткой, имеет плотность около 2,70 г/см³.
Химический состав металла также влияет на его плотность. Так, наличие различных примесей или легирующих элементов может повлиять на структуру металла и, следовательно, на его плотность. Например, добавление никеля к железу для создания нержавеющей стали увеличивает его плотность и делает его более устойчивым к коррозии.
Кроме того, плотность металлов может изменяться при изменении температуры. В зависимости от температуры, молекулярная и атомная структура металла может меняться, что приводит к изменению его плотности. Это свойство используется, например, при производстве биметаллических строительных материалов, которые изменяют свою форму при нагреве или охлаждении.
Влияние физических и структурных особенностей на свойства металлов
Физические и структурные особенности имеют значительное влияние на свойства металлов. Металлы обладают плотностью, которая является одним из их основных свойств. Плотность металлов определяется их атомной и кристаллической структурой.
Атомы металлов обычно имеют небольшой размер и высокую плотность заряда, что обусловлено наличием большого количества электронов уровней d и f. Это позволяет атомам металлов тесно упаковываться в кристаллической решетке и образовывать плотные структуры.
Кристаллическая структура металлов обладает характерной решеткой, в которой атомы занимают узлы. Эта решетка обеспечивает прочность и плотность металла. Внутри кристаллической структуры металла атомы связаны ковалентными и металлическими связями, которые обеспечивают высокую прочность и электропроводность.
Структура металлов также оказывает влияние на их пластичность и способность к деформации. Благодаря своей кристаллической структуре, металлы могут подвергаться пластической деформации без разрушения. Их атомы могут перемещаться в плоскостях характерных для каждого металла, что позволяет им сохранять целостность и форму при деформации.
Таким образом, физические и структурные особенности металлов приводят к их плотности, прочности, электропроводности и пластичности. Эти свойства делают металлы одними из наиболее важных и широко используемых материалов в различных сферах нашей жизни.
Применение плотных металлов в различных отраслях промышленности

Авиационная промышленность: Плотные металлы, такие как титан, вольфрам и никель, широко используются в авиационной промышленности. Титановые сплавы обладают высокой прочностью при небольшом весе, что позволяет уменьшить массу судов и повысить их эффективность. Вольфрам используется для изготовления компонентов реактивных двигателей, благодаря своей высокой температурной стойкости. Никель, в свою очередь, применяется для производства лопаток турбин, благодаря своим механическим свойствам и способности сохранять прочность при высоких температурах.
Энергетическая промышленность: В энергетической промышленности плотные металлы используются для создания компонентов с высокой теплопроводностью и высокой температурной стойкостью. Например, вольфрам применяется для изготовления электродов в термоядерных реакторах и дуговых лампах, так как он обладает высокой температурной стойкостью и низкой теплопроводностью. Кобальтовые сплавы широко применяются в изготовлении магнитов для генераторов и электродвигателей.
Машиностроение: В машиностроении плотные металлы находят широкое применение благодаря своей прочности и значительной твердости. Вольфрамовые и молибденовые сплавы используются для создания инструментального оборудования, такого как сверла, фрезы и резцы. Такие сплавы обеспечивают долговечность и высокую стойкость к износу при обработке различных материалов. Также плотные металлы применяются при изготовлении качественных металлических конструкций и деталей, которые должны быть прочными и надежными.
Медицина: Плотные металлы, такие как платина и золото, используются в медицине для создания имплантатов, протезов и стоматологических изделий. Платиновые сплавы, например, обладают высокой коррозионной стойкостью и химической инертностью, что делает их идеальными для использования внутри организма. Золото, в свою очередь, отличается нежными эстетическими свойствами, из-за чего широко применяется в стоматологии для изготовления протезов и коронок.
Вопрос-ответ

Почему металлы являются плотными?
Металлы являются плотными из-за их структурных и физических особенностей. Одной из основных причин является их кристаллическая структура. В большинстве металлов атомы сгруппированы в регулярные фиксированные решетки, что приводит к образованию компактного и уплотненного материала. Кроме того, межатомные связи в металлах являются сильными и упругими, что также способствует плотности материала.
Какие структурные особенности влияют на плотность металлов?
Существует ряд структурных особенностей, которые влияют на плотность металлов. Одна из них - наличие кристаллической структуры. В большинстве металлов атомы упорядочены в регулярные решетки, что приводит к компактности материала. Кроме того, размер и форма атомов также влияют на плотность металлов. Например, если атомы имеют более большой размер или более сферическую форму, то материал будет плотнее.
